كيفية تسمية المركبات الأيونية
مؤلف:
Roger Morrison
تاريخ الخلق:
5 شهر تسعة 2021
تاريخ التحديث:
1 تموز 2024

المحتوى
- مراحل
- الطريقة الأولى اسم المركبات الأيونية الثنائية
- الطريقة الثانية: اسم المركبات التي تحتوي على معدن انتقالي
- الطريقة الثالثة: اسم المركبات التي تحتوي على أيون متعدد الذرات
تتكون المركبات الأيونية من أيونات المعادن الموجبة (الكاتيونات) والأيونات السالبة غير الأيونية (الأنيونات). للعثور على اسم مركب أيوني ، يجب أولاً العثور على اسم العنصر غير المعدني (العنصر الأيمن) بال لاحقة الصحيحة (-أكل ، أكل ...) ، ثم اسم المعدن المدمج (عنصر اليد اليسرى) ، ولكن بدون لاحقة. بالنسبة للمركبات ذات الفلزات الانتقالية ، تظل القاعدة كما هي ، مع بعض المتغيرات الصغيرة.
مراحل
الطريقة الأولى اسم المركبات الأيونية الثنائية
-

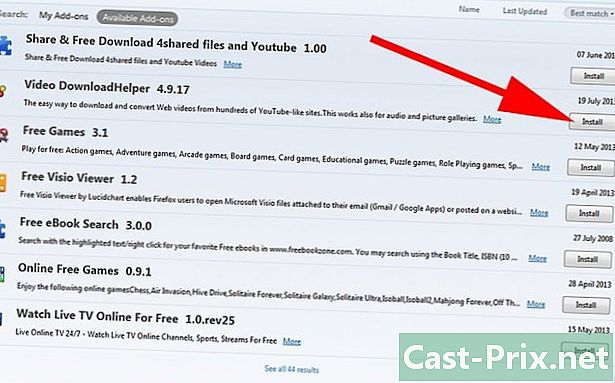
راجع الجدول الدوري للعناصر. جميع العناصر الكيميائية المعروفة موجودة في جدول دوري. يتكون المركب الأيوني الثنائي من معدن (الكاتيون) وغير (الأنيون). هذه ليست عمومية ، ولكن العناصر القادرة على الحصول على الإلكترونات (الأنيونات) هي على يمين الطاولة ، الكاتيونات ، إلى حد ما اليسار. يتم ترك المعادن إلى حد ما ووسط الجدول.- تنتمي الأنيونات في أغلب الأحيان إلى مجموعات 15 أو 16 أو 17 من الجدول الدوري. تميز العائلات المختلفة للعناصر بألوان موضحة في الأسطورة.
- إذا لم يكن لديك هذا الجدول في متناول اليد ، فستجده بسهولة على الإنترنت ، على سبيل المثال في هذا الموقع.
-

أدخل صيغة مركب الأيونية مع اسم غير معروف. افترض أنك مطالب بإعطاء اسم المركب الأيوني للصيغة كلوريد الصوديوم. حسب الظروف ، قيد التقدم ، سوف تكتبه على دفتر الملاحظات أو على السبورة.- هذا المثال معروف جيدًا ، لكنه يسمح بفهم مبدأ التسمية: كلوريد الصوديوم لديه اثنين من الأيونات فقط ولا يحتوي على معدن الانتقال.
-

أدخل اسم المعدن. الجزء الثاني من اسم المركب هو في الواقع اسم المعدن ، العنصر الذي يأتي أولاً في الصيغة ، العنصر الموجب الشحنة (الموجبة). يسبق هذا المعدن الكلمة من (كلوريد من الصوديوم). في الجدول الدوري للعناصر ستجد هذا الرمز نا هو أن الصوديوم ، لذلك وضعت في المركز الثاني.- القاعدة غير قابلة للتغيير: اسم المعدن دائمًا في الموضع الثاني ، بينما يكون رمزه هو الأول في الصيغة.
-

أدخل اسم غير المعدنية مع لاحقة. في حالة أنيون بسيط ، يجب عليك إضافة -ure في جذر العنصر. في مثالنا ، لدينا lanion الكلورينالمجمع هو الكلورلدى عودتهمل الكلورين هو الكلور. في بعض الأحيان يكون الأمر أكثر تعقيدًا: لذا ، عندما يكون اللازوت على المحك ، لا نتحدث عن الأزيد ، ولكن عن النتريد.- مبدأ المذهب بالنسبة للعديد من Danions لا يزال دون تغيير. لذلك ، في أي مركب أيوني يحتوي على الفوسفور ، سيكون لديك فوسفيد ... وإذا كان هناك ليود ، يوديد من ...
-

تجميع بالترتيب الصحيح أسماء lanion والكاتيون. بمجرد العثور على أسماء الجزأين من المركب الأيوني ، تكون بعيدًا عن الهدف. يجب أن يتم تجميعها في ترتيب الأيونات الموجبة ، والتي ل كلوريد الصوديوم سوف تعطي كلوريد الصوديوم . -

تدرب مع المركبات الأيونية البسيطة الأخرى. لقد رأينا للتو حالة معروفة من كلوريد الصوديوم ، ولكن هناك العديد من المركبات الأخرى من هذا النوع. يجب الاحتفاظ ببعضها لتكون بمثابة نماذج للمركبات التي تتم مواجهتها في كثير من الأحيان. مع هذه المركبات ، ليست هناك حاجة للنظر في عدد dions المعنية. كتمرينات ، حاول العثور على أسماء المركبات التالية (الإجابة تكون مرئية إذا حددت المساحة الفارغة بعد العلامة "="):- لي2S = كبريتيد الليثيوم
- حج2S = كبريتيد الفضة
- MgCl2 = كلوريد المغنيسيوم
الطريقة الثانية: اسم المركبات التي تحتوي على معدن انتقالي
-

أدخل صيغة المركب الأيوني. دعونا نأخذ على سبيل المثال المركب الذي له الصيغة: Fe2O3. توجد معادن الانتقال في الجزء المركزي من الجدول الدوري وعلى الأسطر الأربعة ، ستجد ، على سبيل المثال ، البلاتين والذهب والزركونيوم ... للعثور على اسم المركب ، يجب أن تأخذ في الاعتبار تحميله ، المبلغ عنه برقم روماني.- تكون مركبات الفلزات الانتقالية دائمًا أكثر حساسية لبعض الشيء لأن عدد الأكسدة (شحنة) الأخير قد يختلف تبعًا للتفاعل.
-

تحديد تحميل المعادن الأسد. إذا كان المعدن قيد التشغيل ينتمي على الأقل إلى المجموعة 3 من الجدول الدوري ، فيجب أن تشعر بالقلق إزاء عدد الأكسدة. يشير lanion lindice الذي يرتبط به المعدن إلى شحنة المعدن الانتقالي. سيكون للمعادن شحنة موجبة وفي حالتنا ، يكون للأكسجين دائمًا شحنة -2 ، ذرات الثلاث O3 نفترض أن هناك 6 إلكترونات لتحقيق التوازن. لأن هناك اثنين من ذرات الحديد في الحديدوخلص بالتالي إلى أن الحمل الحديد هنا هو +3.- يمكنك أيضًا القيام بالعكس من خلال كتابة أن أسد الأكسجين له شحنة -2.
- بشكل عام ، في التدريبات المدرسية ، يتم ذكر كميات كلا العنصرين إما في الصيغة أو في البيان.
-

العثور على اسم المعدن. سوف تضيف شحنة له في الأرقام الرومانية. إذا لزم الأمر ، ابحث عن اسم الكاتيون (المعدن) في الجدول الدوري. الحديد هو رمز الحديد وله شحنة موجبة من +3 ، سوف تضطر إلى الكتابة ... الحديد (الثالث) .- يتم استخدام الأرقام الرومانية فقط في المذهب. في أي حال من الأحوال لا تظهر في الصيغ أو ردود الفعل.
-

العثور على صياغة الصحيح من غير المعادن. يجب العثور على لاحقة. إذا لزم الأمر ، ابحث عن اسم lanion في الجدول الدوري. هذه هي الطريقة الأكسجين (O) هي حالة خاصة: إنها تفقد نهايتها -Gene لمصلحة من -من، يعطي أكسيد .- من ناحية أخرى ، تأخذ جميع الأنيونات الأخرى إنهاء في -ure. بوضوح ، أيا كان المعدن المرتبط ، يتم تعيين الأنيونات دائمًا بنفس الطريقة.
-

الجمع بين أسماء العنصرين. لا تختلف هذه العملية عما رأيناه بمركبات بسيطة. تجميع عنصرين التسميات المحددة سابقا ، ناهيك عن الأرقام الرومانية. هذه هي الطريقة الحديد2O3 هو منأكسيد الحديد (III) . -

تعرف الطوائف القديمة. في الماضي ، لم تستخدم الأرقام الرومانية للمعادن التي تمر بمرحلة انتقالية -eux أو في -ique. راقب عن كثب جزأين من المركب الأيوني. إذا كان للأسد المعدني شحنة أقل من الأسد غير المعدني ، فسوف تستخدم النهاية -eux. إذا كان العكس ، فسوف تستخدم النهاية في -ique .- Fe لديه شحنة أقل من الأكسجين (Fe لديه شحنة أعلى) ، بحيث يعطي الحديد هنا الهدف حديدي. لذلك ، FeO هو منأكسيد الحديد.
- الطوائف حديدي و حديدي وبالتالي لديهم نفس الجذر بالنظر إلى ما يشير كلاهما إلى العنصر الحديد.
-

لا تستخدم الأرقام الرومانية مع بعض المركبات. هذه هي الحالة التي تحتوي على الزنك أو الفضة.دائمًا ما يكون لهذين المعدنين ، بغض النظر عن التفاعل الكيميائي ، نفس عدد الأكسدة ، بحيث لا يوجد سوى فئة واحدة: الزنك دائمًا له شحنة +2 ، في حين أن الفضة لها دائمًا شحنة بقيمة +1.- هذا يعني أن المركبات التي تحتوي على هذه العناصر تكون دائمًا من النوع "... zinc" أو "... silver". لن ترى الأرقام الرومانية معًا.
الطريقة الثالثة: اسم المركبات التي تحتوي على أيون متعدد الذرات
-

أدخل صيغة أيون متعدد الذرات الخاص بك. بحكم التعريف ، يحتوي هذا المركب الأيوني عدة أيونات مجتمعة بطرق مختلفة. بشكل عام ، يوجد كاتيون واحد (معدن) وأنيون (غير معدني) ، يتكون من عدة ذرات. إذا كنت لا تعرف أسماء الأيونات ، فارجع إلى الجدول الدوري. لنأخذ مثالًا كلاسيكيًا ، مركب الصيغة FeNH4(SO4)2 . -

تحديد تهمة المعادن الأسد. أولا ، الأسد SO4 لديه تهمة -2. ال 2 في مؤشر SO4 يشير إلى أن هناك اثنين من هذه الأيونات في المجمع. وهذا ما يسمى ايون كبريتاتلأنه مزيج من الأكسجين والكبريت. لذلك الحمل هو: 2 × -2 = -4. من جانبها ، أسد الأمونيوم NH4 (مع 1 ذرة من النيتروجين و 4 من الهيدروجين) لديه تهمة +1. غاز غاز الأمونيا صيغة NH3 مستقرة ولديها شحنة محايدة ، ولكن إذا تمت إضافة ذرة الهيدروجين إليها ، فإنها تصبح NH4 بتهمة +1. كبريتات الأمونيوم (NH4(SO4)2 لذلك يحتوي على تحميل: -4 + 1 أو -3. وهذا يعني أن الأسد الحديدي (الحديد) يجب أن يكون هناك رسوم +3 لكي يكون المجمع ثابتًا.- المركبات الأيونية لها شحنة محايدة ، وإلا فإنها لن تكون مستقرة. بفضل هذه الخاصية يمكنك أن تجد حمولة الأسد المعدني.
- أسد4 له شحنة -2 وعندما يتم دمجها مع ذرتين هيدروجين ، يحمل كل منهما شحنة -1 ، يصبح مركبًا ثابتًا: حمض الكبريتيك من الصيغة H2SO4 .
-

اسم أيون المعادن. هناك طريقتان للقيام بذلك: الطريقة القديمة والطريقة الجديدة ، حتى لو بدأت حتى الآن. في حالة Fe2O3، يمكنك أن تقول أنه أكسيد الحديديك (الاسم القديم) أو من أكسيد الحديد (III) (طائفة جديدة). -

أدخل الاسم العالمي للأيونات غير المعدنية. من خلال قراءة الجدول الدوري ، سوف تكتشف هذا الرمز S يتوافق مع الكبريت ويتحد مع الأكسجين في شكل SO4هو يصبح كبريتات. وبالمثل ، عندما يتم دمج ذرة النيتروجين مع 4 ذرات هيدروجين (NH4) ، كله أسد الأمونيوم. أخيرًا ، من خلال الجمع بين الاثنين ، سيكون لديك كبريتات الأمونيوم.- غاز غاز الأمونيا، وجود شحنة محايدة ، يصبح أسد الأمونيوم إذا تم إضافة أيون إيجابي إليها.
- اربط أسماء المعدن بأسماء المعادن اللافلزية. هذا هو FeNH4(SO4)2 هو من كبريتات الأمونيوم والحديد (الثالث).

- باسم سابق ، يسمى هذا المركب كبريتات الأمونيوم الحديديك.